广东工业大学 分析测试中心 510006
摘要:近红外光谱(NIR)归属于分子振动的倍频、合频光谱,具有丰富的结构和组成信息,是近些年来快速发展的高新应用技术之一。近红外光有更好的聚焦深度、生物组织穿透能力以及较小的细胞损伤等优势,适合生物、防伪等领域的应用。同时,近红外光作为太阳光谱的一部分,在光催化、光降解、光化学反应等方面具有重要的研究价值。目前,实验中所用溶剂的紫外截止波长比较容易查找,但不同溶剂的近红外吸收研究较少,实验前需要查阅大量文献,或购买多种不同溶剂进行筛选,经济和时间成本较大。为此,本文用紫外可见近红外分光光度计测试了19种常见溶剂的近红外吸收光谱,并对谱图进行归属,希望能为科研工作者提供一定的信息参考。
关键词:近红外吸收;分光光度计;吸收光谱;溶剂
引言:
近红外光是介于可见光和中红外光之间的电磁波,近红外光的波长范围约为780~2500 nm,对应频率范围是12820~4000 cm-1。紫外或可见光在许多介质中的穿透能力有限,尤其是生物组织,对可见光的吸收非常强,大大限制了其在生物领域的应用。近红外光,相比于紫外或可见光,具有较好的穿透能力,即使是在复杂的生物组织——含有糖类、核酸、蛋白质等多种组分的体系,也具有相当可观的穿透深度,因而越来越多的应用于医学诊断或治疗方面[1 ~ 3]。
研究表明,近红外光在生物组织中的穿透深度可达数厘米,由于组织的光学穿透效率高,自发荧光少,早期人们将700-900 nm波长范围称作肿瘤的“光治疗窗口”,近红外光学层析成像也在逐步得到应用。近些年来,为满足现代生物医学的需求,用于检验检测的仪器不断提升,使得近红外第二窗口(NIRⅡ,1000-1700 nm)成像技术得以发展和应用。张晓兵课题组合成了一类量子产率高、性能稳定、斯托克斯位移大的聚甲基胺染料(NIRⅡ-RTs),其中NIRⅡ-RT3和NIRⅡ-RT4可制备成高信噪比的NIRⅡ生物成像探针,并实现了药物诱导的肝毒性实时监测[4]。
Ag2E(E= S, Se 或Te)体相材料通常具有较窄的带隙, 理论上其量子点发光光谱出现在近红外第二窗口[5~7]。庞代文课题组以巯基辛烷作为表面配体,通过调控Ag前体和Te前体的比例,制备出油溶性的Ag2Te 量子点,该纳米颗粒粒径均匀、分散性好、吸收波长和发射峰波长都红移至近红外第二窗口。且该Ag2Te 量子点不含有毒金属,制备简单,荧光性能优异,适合于生物活体成像,因而在生物成像方面具有良好的应用前景[8]。Ellen M. Sletten和Oliver T. Bruns等设计合成了一系列短波红外(SWIR, 1000-2000 nm)聚甲基胺荧光团,建立了SWIR造影剂的结构和光物理性质之间的关系。光学造影剂的设计和生物成像技术的互补,实现了实时、无创的动物多色成像技术。优化后的染料匹配到980 nm和1064 nm激光,结合吲哚菁绿,实现实时、高时间和空间分辨率的三色成像[9]。
近红外光谱反应的是发生在中红外区的分子基频产生的一系列倍频和组合频吸收的特征。用于溶液样品吸收性质测试的溶剂有很多种,不同溶剂紫外截止波长的数据比较容易获取,但近红外波段的吸收数据不多。而很多溶剂具有含氢基团,X-H键伸缩和弯曲基频振动会产生一系列倍频和组合频,可能会对样品性质的测定产生一定的影响。为此,本文测定了19种常见溶剂的近红外吸收谱图,以供科研工作者参考。
1实验部分
1.1仪器与试剂
使用UV3600 plus紫外可见近红外分光光度计(岛津制作所)。
纯水,甲醇(分析纯,天津大茂),乙醇(分析纯,天津大茂),乙腈(分析纯,麦克林),乙醚(分析纯,阿拉丁),丙酮(分析纯,麦克林),1,4-二氧六环(≥99.0%,迈瑞尔),正己烷(分析纯,stream power),环己烷(分析纯,天津大茂),乙酸(分析纯,麦克林),乙酸乙酯(分析纯,麦克林),二氯甲烷(分析纯,麦克林),三氯甲烷(分析纯,麦克林),苯(分析纯,麦克林),甲苯(分析纯,阿拉丁),石油醚(分析纯,麦克林),N’N-二甲基亚砜(分析纯,阿拉丁),N’N-二甲基甲酰胺(分析纯,阿拉丁),四氢呋喃(分析纯,阿拉丁),四氯乙烯(红外分析用,麦克林),以上试剂均为商业购买,未经纯化或其他处理。
1.2测定步骤
采用1cm光程的石英比色皿,以空气为基线,在紫外可见近红外分光光度计上测试19种溶剂的近红外波段的吸收谱图。
2结果与讨论
近红外光谱的波长范围是780~2500 nm,对应的频率范围是12820~4000 cm-1。该波段范围承载的主要信息是含氢基团振动的倍频和组合频的特征信息。表1-1汇总了主要含氢基团合频与各级倍频吸收带的频率约值[10] 。
表1-1 主要含氢基团合频与各级倍频吸收带的频率约值
C-H | N-H | O-H | H2O | C-H | N-H | O-H | H2O | |
振动类型 | 频率/cm-1 | 波长/nm | ||||||
伸缩基频 | 3000 | 3300 | 3600 | 3300 | 3000 | 2700 | ||
剪式弯曲 | 1450 | 1550 | 1500 | 6700 | 6452 | 6250 | ||
合频 | 4250 | 4650 | 5000 | 5155 | 2350 | 2150 | 2000 | 1940 |
二倍频 | 5800 | 6670 | 6700 | 6940 | 1720 | 1500 | 1450 | 1440 |
三倍频 | 8480 | 9520 | 10500 | 10420 | 1180 | 1050 | 950 | 960 |
四倍频 | 11100 | 12500 | 13500 | 13300 | 900 | 800 | 740 | 750 |
五倍频 | 13300 | 750 | ||||||
注:υ-基频,2υ-二倍频即基频的一级倍频,3υ-三倍频,4υ-四倍频,5υ-五倍频
水的近红外吸收谱图如图1所示。O-H伸缩振动基频(υ)约为2700 nm,剪式弯曲振动基频约为6250 nm。其中840 nm的吸收峰归属于2υ1+υ2+υ3,970 nm附近的吸收峰归属于2υ1+υ3,1160 nm附近的吸收峰归属于υ1+υ2+υ3,1460 nm附近的宽峰归属于υ1+υ3,1900 nm及以上的强的吸收峰是水分子反对称伸缩振动和弯曲振动的组合频谱带[11~12]。当用水做基线,测试其谱图,如图1b,我们发现,1400 nm以下的组合频吸收可以通过基线扫描的方式减弱。但1400 nm以上,由于水的吸收很强,几乎将1400 nm以上的光全部吸收,此时,当我们将样品溶解到水中以后,由于吸光度具有加和性,实际谱图反映的是溶剂和样品的总的吸收信号,溶剂已经将光信号吸收的情况下,这样就无法测试到准确的样品吸收信号。
 a
a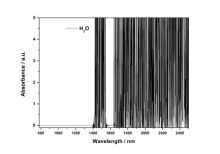 b
b
图1 水的近红外吸收光谱
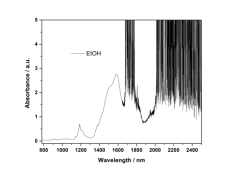
甲醇和乙醇的近红外吸收谱图如图2所示。O-H伸缩振动基频(υ)约为2700 nm,剪式弯曲振动基频约为6250 nm。C-H的伸缩振动基频(υ)约为3300 nm,剪式弯曲振动基频约为6452 nm。图2a中甲醇在915 nm处的吸收峰和图2c中乙醇在908 nm处的吸收峰归属于甲基C-H伸缩振动的三级倍频,甲醇在1026 nm和乙醇1015 nm处的吸收峰归属于O-H伸缩振动的一级倍频和三倍的C-O伸缩振动的组合频;甲醇1200 nm和乙醇1187 nm处的吸收峰归属于能够形成氢键的体系中的O-H的一级倍频;1400-1700 nm之间的一系列吸收峰主要归属于不同聚合体的O-H伸缩振动的一级倍频,如甲醇或乙醇的单体,二聚体、多聚体等,C-H和O-H的组合频也有一定的贡献;1700-1900 nm是O-H伸缩振动和O-H弯曲振动的组合频;1900 nm以上,归属于O-H伸缩振动和C-H弯曲振动的组合频,O-H伸缩振动和O-H弯曲振动的组合频以及O-H伸缩振动和C-O伸缩振动的组合频。同样,图2b和2d,1650-1800 nm波段和2000-2500 nm波段,甲醇或乙醇几乎将光信号全部吸收,无法区分该区域的样品信号。
 a
a b
b
 c
c d
d
图2 甲醇和乙醇的近红外吸收光谱
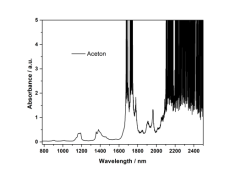
乙腈和丙酮的近红外吸收谱图如图3所示。C-H的伸缩振动基频(υ)约为3300 nm,剪式弯曲振动基频约为6452 nm。图3a中,乙腈在894 nm和1005 nm处的吸收峰归属于甲基C-H伸缩振动的三级倍频和第三组合频;1173 nm和1320-1512 nm处的吸收峰归属于甲基C-H伸缩振动的二级倍频和第二组合频;1600-1800 nm和2200-2500 nm的吸收峰为C-H伸缩振动的一级倍频和第一组合频。图3b中,丙酮在894 nm和1016 nm处的吸收峰归属于甲基C-H伸缩振动的三级倍频和第三组合频;1176 nm和1323-1506 nm处的吸收峰归属于甲基C-H伸缩振动的二级倍频和第二组合频;1600-1800 nm和2100-2500 nm的吸收峰为C-H伸缩振动的一级倍频和第一组合频。图3b和图3d,分别以乙腈或丙酮做基线,再测试溶剂的吸收,发现一级倍频和第一组合频的吸收很强,这些波段不适合对样品进行吸收分析。
 a
a b
b
 c
c d
d
图3 乙腈和丙酮的近红外吸收光谱
乙酸和乙酸乙酯的近红外吸收谱图如图4所示。图4a中乙酸在900 nm和1010 nm处的吸收峰归属于甲基和亚甲基的C-H伸缩振动的三级倍频和第三组合频;1169 nm和1325-1512 nm处的吸收峰归属于甲基和亚甲基的C-H伸缩振动的二级倍频和第二组合频; 1400-1700 nm之间的一系列吸收峰主要归属于不同聚合体的O-H伸缩振动的一级倍频,如乙酸的单体,二聚体、多聚体等,C-H和O-H的组合频也有一定的贡献;1700-1900 nm是O-H伸缩振动和O-H弯曲振动的组合频;1900 nm以上,归属于O-H伸缩振动和C-H弯曲振动的组合频,O-H伸缩振动和O-H弯曲振动的组合频以及O-H伸缩振动和C-O伸缩振动的组合频。同样,如图4b,1650-2500 nm波段,乙酸几乎将光信号全部吸收,加入样品后,无法区分该区域的样品信号。图4c中乙酸乙酯在903 nm和1010 nm处的吸收峰归属于甲基C-H伸缩振动的三级倍频和第三组合频;1180 nm和1320-1500 nm处的吸收峰归属于甲基和亚甲基的C-H伸缩振动的二级倍频和第二组合频;1660-1800 nm和2000-2500 nm的吸收峰为C-H伸缩振动的一级倍频和第一组合频。如图4d,乙酸乙酯在C-H伸缩振动的一级倍频和第一组合频的区域将光信号全部吸收,该区域不适合用于分析样品的光吸收性质。
 a
a b
b
 c
c d
d
图4 乙酸和乙酸乙酯的近红外吸收光谱
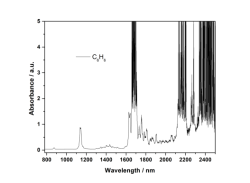
苯和甲苯的近红外吸收谱图如图5所示。图5a中,苯在874 nm处的吸收峰归属为苯环C-H伸缩振动的三级倍频,1137 nm处的吸收峰归属为C-H伸缩振动的二级倍频;1143 nm处的吸收峰归属为两倍的C-H伸缩振动和C-C弯曲振动的组合频;1600-1900 nm和2000-2500 nm处的吸收峰归属于对称和反对称的C-H伸缩振动的一级倍频和第一组合频。图5c甲苯在867 nm处的吸收峰归属于苯环C-H伸缩振动的三级倍频;1142 nm处的吸收峰归属为苯环两倍的C-H伸缩振动和C-C弯曲振动的组合频C-H伸缩振动的二级倍频;912 nm和1016 nm处的吸收峰归属于甲基的C-H伸缩振动的三级倍频和第三组合频; 1191 nm处的吸收峰和1320-1500 nm处的吸收峰归属于甲基的C-H伸缩振动的二级倍频和第二组合频;1600-1880 nm和2100-2500 nm的吸收峰为C-H伸缩振动的一级倍频和第一组合频。图5b和图5d所示,苯和甲苯的C-H伸缩振动一级倍频和第一组合频吸收波段,不适合用于样品吸收性质的分析。
 a
a  b
b
 c
c  d
d
图5 苯和甲苯的近红外吸收光谱
二氯甲烷和氯仿的近红外吸收谱图如图6所示。图6a中二氯甲烷在884 nm处的吸收峰归属为亚甲基C-H伸缩振动的三级倍频;1155 nm和1330-1500 nm处的吸收峰归属于亚甲基的C-H伸缩振动的二级倍频和第二组合频;1650-1750 nm和2200-2500 nm的吸收峰为C-H伸缩振动的一级倍频和第一组合频;图6c氯仿在884 nm处的吸收峰归属为次甲基C-H伸缩振动的三级倍频;1215 nm和1411 nm处的吸收峰归属于次甲基的C-H伸缩振动的二级倍频和第二组合频;1675-1725 nm和2250-2500 nm的吸收峰为次甲基C-H伸缩振动的一级倍频和第一组合频; 图6b和图6d中,二氯甲烷或氯仿的C-H伸缩振动的一级倍频和第一组合频吸收区,不适用于进行样品的吸收性质分析。
 a
a b
b
 c
c  d
d
图6 二氯甲烷和氯仿的近红外吸收光谱
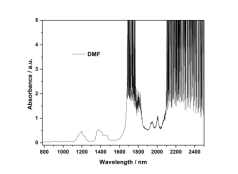
N’N-二甲基甲酰胺和二甲基硫砜的近红外吸收谱图如图7所示。图7a中N’N-二甲基甲酰胺在915 nm和1013 nm处的吸收峰归属于甲基C-H伸缩振动的三级倍频和第三组合频;1100-1300 nm和1330-1500 nm处的吸收峰归属于甲基的C-H伸缩振动的二级倍频和第二组合频;1600-1900 nm和2000-2500 nm的吸收峰为C-H伸缩振动的一级倍频和第一组合频。如图7c中二甲基硫砜901 nm和1010 nm处的吸收峰归属于甲基C-H伸缩振动的三级倍频和第三组合频;1100-1300 nm和1350-1500 nm处的吸收峰归属于甲基的C-H伸缩振动的二级倍频和第二组合频;1600-1900 nm和2000-2500 nm的吸收峰为C-H伸缩振动的一级倍频和第一组合频。图7b和图7d中,DMF或DMSO的C-H伸缩振动的一级倍频和第一组合频吸收波段,不适用于进行样品吸收性质的解析。
 a
a  b
b
 c
c  d
d
图7 N’N-二甲基甲酰胺和二甲基硫砜的近红外吸收光谱
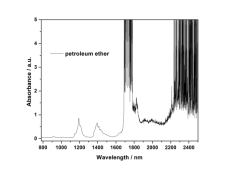
正己烷、环己烷和石油醚的近红外吸收谱图如图8所示。图8a中正己烷在924 nm和1013 nm处的吸收峰归属于甲基和亚甲基C-H伸缩振动的三级倍频和第三组合频;1130-1280 nm和1350-1550 nm处的吸收峰归属于甲基和亚甲基的C-H伸缩振动的二级倍频和第二组合频;1670-1900 nm和2200-2500 nm的吸收峰为甲基和亚甲基C-H伸缩振动的一级倍频和第一组合频。图8c中环己烷在914 nm和1013 nm处的吸收峰归属于亚甲基C-H伸缩振动的三级倍频和第三组合频;1150-1280 nm和1360-1500 nm处的吸收峰归属于亚甲基的C-H伸缩振动的二级倍频和第二组合频;1690-1900 nm和2200-2500 nm的吸收峰为亚甲基C-H伸缩振动的一级倍频和第一组合频。图8e中石油醚在913 nm和1019 nm处的吸收峰归属于亚甲基C-H伸缩振动的三级倍频和第三组合频;1150-1250 nm和1360-1500 nm处的吸收峰归属于甲基和亚甲基的C-H伸缩振动的二级倍频和第二组合频;1660-1900 nm和2200-2500 nm的吸收峰为甲基和亚甲基C-H伸缩振动的一级倍频和第一组合频。图8b、图8d和图8f中,正己烷、环己烷或石油醚的C-H伸缩振动的一级倍频和第一组合频吸收波段,不适用于进行样品吸收性质的解析。
 a
a b
b
 c
c d
d
 e
e  f
f
图8 正己烷、环己烷和石油醚的近红外吸收光谱
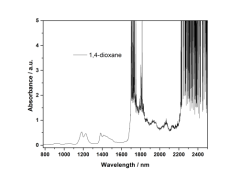
1,4-二氧六环、四氢呋喃和四氯乙烯的近红外吸收谱图如图9所示。其中图9a中1,4-二氧六环在907 nm和1016 nm处的吸收峰归属于亚甲基C-H伸缩振动的三级倍频和第三组合频;1184 nm、1280 nm和1350-1500 nm处的吸收峰归属于亚甲基的C-H伸缩振动的二级倍频和第二组合频;1670-1900 nm和2200-2500 nm的吸收峰为甲基和亚甲基C-H伸缩振动的一级倍频和第一组合频。图8c中环己烷在914 nm和1013 nm处的吸收峰归属于亚甲基C-H伸缩振动的三级倍频和第三组合频;1206 nm和1360-1500 nm处的吸收峰归属于亚甲基的C-H伸缩振动的二级倍频和第二组合频;1700-1900 nm和2200-2500 nm的吸收峰为亚甲基C-H伸缩振动的一级倍频和第一组合频。图9b和图9d中,1,4-二氧六环或四氢呋喃的C-H伸缩振动的一级倍频和第一组合频吸收波段,不适用于进行样品吸收性质的解析。图9e为四氯乙烯的近红外吸收谱图,四氯乙烯在整个近红外区域没有吸收。
 a
a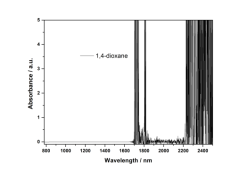 b
b
 c
c d
d
 e
e
图9 1,4-二氧六环、四氢呋喃和四氯乙烯的近红外吸收光谱
综上,我们可以看出,一般C-H或O-H伸缩振动的一级倍频和第一组合频的吸收很强,几乎将光线全部吸收,这两个波段几乎没有光线能够进到检测器。这种情况下,无法区分是待测物的吸收还是溶剂的吸收。可以选用不含氢的四氯乙烯做溶剂,进行样品吸收信号的分析。
3结论
本文利用紫外可见近红外分光光度计测试了19种常见溶剂的吸收谱图,并对谱图进行归属,除四氯乙烯外,其他18种常见溶剂在近红外波段都有比较强的吸收。因此,测试溶液状态下的近红外吸收谱图,可以尝试样品是否能溶解于四氯乙烯,此外,为减小溶剂对样品近红外吸收的影响,尽量选取光程小(如1mm)的比色皿,或采用混合溶剂,达到稀释的目的,从而准确获取样品的吸收信息。
参考文献:
1.Sun Y. Q., Sun P. J., Li Z. H., Qu L. B., Guo W., Chem. Soc. Rev., 2022, 51, 7170-7205.
2.Dong B. H. , Li C. Y. , Chen G. C. , Zhang Y. J. , Zhang Y. , Deng M. J. , Wang Q. B. , Chem. Mater. , 2013, 25(12), 2503-2509.
3.Zhou J., Rao L., Yu G. C., Cook T. R., Chen X. Y., Huang F. H., Chem. Soc. Rev., 2021,50, 2839-2891.
4.Ren T. B., Wang Z. Y., Xiang Z., Lu P., Lai H. H., Yuan L., Zhang X. B., Tan W. H.,Angew. Chem. Int. Ed.,2021, 60, 800-805.
5.Du Y. P. , Xu B. , Fu T. , Cai M. , Li F. , Zhang Y. , Wang Q. B. , J. Am. Chem. Soc. , 2010, 132(5), 1470-1471.
6.Jiang P. , Tian Z. Q. , Zhu C. N. , Zhang Z. L. , Pang D. W. , Chem. Mater. , 2012, 24(1), 3-5.
7.Gu Y. P. , Cui R. , Zhang Z. L. , Xie Z. X. , Pang D. W. , J. Am. Chem. Soc. , 2012, 134(1) , 79-82.
8.王佳梅, 朱春楠, 朱东亮, 田智全, 林摇 毅, 庞代文, 高等学校化学学报,2015,36(7),1264-1268.
9.Cosco E. D., Spearman A. L., Ramakrishnan S., Lingg Jakob G. P., Saccomano M., PengshungM., Arús B. A., WongK. C. Y.,Glas S., Ntziachristos V., Warmer M., McLaughlin R. R., Bruns O. T., Sletten E. M., Nat Chem, 2020,12,1123-1130.
10.严衍禄, 陈斌, 朱大洲等,《近红外光谱分析的原理、技术与应用》,中国轻工业出版社.
11.Yamatera H., Fitzpatrick B., Gordon G.,J Mol Spectrosc, 1964,14,268-278.
12.Jerry Workman,Jr. Lois Weyer编著,褚小立,许育鹏,田高友译,《近红外光谱解析实用指南》,化学工业出版社
作者:尹少云,女,博士,实验师,主要从事发光功能配合物的研究,E-mail:Sherry_111@gdut.edu.cn
中国高等教育学会高等教育科学研究“十三五”规划课题(2019SYSYB07);广东省省级科技计划项目(2022A0505020005)资助